Agua que cambia de color (Reacciones químicas)
https://youtu.be/EVS7U92VxJ8
Las reacciones químicas pueden ser sorprendentes, como estás
Este experimento se trata de una típica reacción ácido-base. El hidróxido de sodio (también conocido como sosa cáustica o sosa) es una base fuerte, una sustancia que tiene la capacidad de tomar un protón fácilmente. Cuando se mezcla con un ácido, se forma una sal y agua en la reacción de neutralización. Podemos escribir la siguiente reacción general de neutralización:
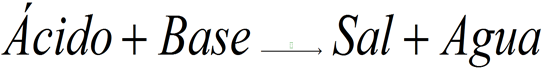
Para este caso en particular, lo que tenemos es a la fenolftaleína actuando como ácido. Se preguntarán ¿qué es la fenolftaleína? La fenolftaleína es una sustancia química que tiene la particularidad de tener distinta coloración al cambiar entre su forma ácida y su forma básica. La fenolftaleína es una molécula orgánica aromática sustituida en varias posiciones. La coloración rosada que tiene en su forma básica se debe a la conjugación de enlaces dobles que se obtiene al desprotonarse el grupo fenol.

Forma Ácida Forma básica
Incolora Rosada
Al agregar hidróxido de sodio (NaOH) lo que estamos haciendo es desplazar el equilibrio químico hacia la forma básica de la fenolftaleína. La especie reactiva del hidróxido es el ión oxhidrilo (OH- ) que se libera cuando disolvemos el hidróxido de sodio en agua. Por eso es tan importante disolver bien las lentejas del hidróxido. Cualquier base fuerte logra el mismo efecto. Entre las cosas básicas que podemos tener a mano en casa están: los detergentes, la lejía, el carbonato de sodio, cal muerta (hidróxido de calcio), entre otros.
La fenolftaleína es usada normalmente en los laboratorios como indicador ácido-base ya que podemos evidenciar, por el cambio de color, que ocurrió una neutralización en el medio. Debido a su intenso color es posible ponerla en pequeñas cantidades. De este modo cuando se neutralice todo el ácido (por ejemplo HCl, ácido clorhídrico) se neutralizará la pequeña cantidad de fenolftaleína indicando que se llegó al punto final de la neutralización o titulación. Existe una gran cantidad de indicadores ácido base que nos permiten, además de trabajar en el laboratorio, hacer experimentos divertidos.
Las reacciones químicas pueden ser sorprendentes, como estás
Este experimento se trata de una típica reacción ácido-base. El hidróxido de sodio (también conocido como sosa cáustica o sosa) es una base fuerte, una sustancia que tiene la capacidad de tomar un protón fácilmente. Cuando se mezcla con un ácido, se forma una sal y agua en la reacción de neutralización. Podemos escribir la siguiente reacción general de neutralización:
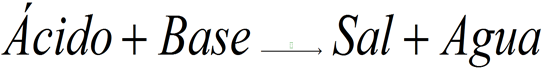
Para este caso en particular, lo que tenemos es a la fenolftaleína actuando como ácido. Se preguntarán ¿qué es la fenolftaleína? La fenolftaleína es una sustancia química que tiene la particularidad de tener distinta coloración al cambiar entre su forma ácida y su forma básica. La fenolftaleína es una molécula orgánica aromática sustituida en varias posiciones. La coloración rosada que tiene en su forma básica se debe a la conjugación de enlaces dobles que se obtiene al desprotonarse el grupo fenol.

Forma Ácida Forma básica
Incolora Rosada
Al agregar hidróxido de sodio (NaOH) lo que estamos haciendo es desplazar el equilibrio químico hacia la forma básica de la fenolftaleína. La especie reactiva del hidróxido es el ión oxhidrilo (OH- ) que se libera cuando disolvemos el hidróxido de sodio en agua. Por eso es tan importante disolver bien las lentejas del hidróxido. Cualquier base fuerte logra el mismo efecto. Entre las cosas básicas que podemos tener a mano en casa están: los detergentes, la lejía, el carbonato de sodio, cal muerta (hidróxido de calcio), entre otros.
La fenolftaleína es usada normalmente en los laboratorios como indicador ácido-base ya que podemos evidenciar, por el cambio de color, que ocurrió una neutralización en el medio. Debido a su intenso color es posible ponerla en pequeñas cantidades. De este modo cuando se neutralice todo el ácido (por ejemplo HCl, ácido clorhídrico) se neutralizará la pequeña cantidad de fenolftaleína indicando que se llegó al punto final de la neutralización o titulación. Existe una gran cantidad de indicadores ácido base que nos permiten, además de trabajar en el laboratorio, hacer experimentos divertidos.



Comentarios
Publicar un comentario